はじめに
2025年8月、東京都内のクリニックで患者の自家脂肪由来幹細胞を点滴する自由診療の再生医療中に患者が急変し、そのまま亡くなるという事故が報じられました。このケースは国内で初めて、自由診療の再生医療による死亡事故として行政が提供停止命令を出した例です。本記事では事故の概要と問題点を整理したうえで、自由診療の再生医療に潜む一般的なリスクについて解説します。
事故の概要と医療安全の問題
何が起こったのか
事故が発生したのは東京都中央区の「東京サイエンスクリニック」(旧称ティーエスクリニック)で、患者自身の脂肪から採取した幹細胞を培養し点滴する治療を自由診療として提供していました。50代の女性が治療を受けた際、点滴中に容体が急変し心停止となり、別病院に搬送されましたが死亡が確認されました。原因は不明であり、厚生労働省は再生医療等安全性確保法に基づき緊急の提供停止命令を出しました。
なぜ問題なのか
この治療では患者自身の細胞を使用していたものの、培養過程での混入物質や試薬により予期せぬ免疫反応が起こる可能性が指摘されました。また、点滴治療はアナフィラキシーや塞栓症といった急変リスクがあり、高度な救命体制が不可欠ですが、一般クリニックでは対応設備や人員が不足しがちです。さらに、治療の有効性を示す十分な医学的根拠がなかったことも課題です。こうした理由から、事故後に細胞加工施設とクリニックに対して提供停止命令が出され、原因究明と再発防止策が求められました。
自由診療の再生医療に潜む問題点
自由診療の再生医療は保険外診療として個人が全額費用を負担する治療で、先端的な治療を早く受けられる可能性がある一方、以下のような課題が知られています。
届出制による規制のゆるさ
日本では再生医療等安全性確保法が2014年に施行され、再生医療を提供する際には医療機関が計画書を第三者委員会で審査のうえ厚生労働省に届出することが義務付けられました。しかしこれは「承認制度」ではなく届出制であり、行政が治療内容を個別に審査・承認しているわけではありません。そのため、あたかも国が承認したかのような広告を行うクリニックも存在し、誤解を招いています。日本再生医療学会は、厚労省が治療法を承認しているかのような広告は虚偽広告であり注意するよう呼びかけています。
治療計画の質のばらつき
京都大学 CiRA の調査によると、2022年末時点で届出された再生医療計画は5,013件が自由診療の計画であり、臨床研究は104件と圧倒的に少数でした。自由診療計画の中には、科学的根拠が乏しいものや担当医師の専門分野と対象疾患が一致しないものが相当数含まれています。下のグラフは自由診療計画の数と臨床研究計画の数を比較したものです。
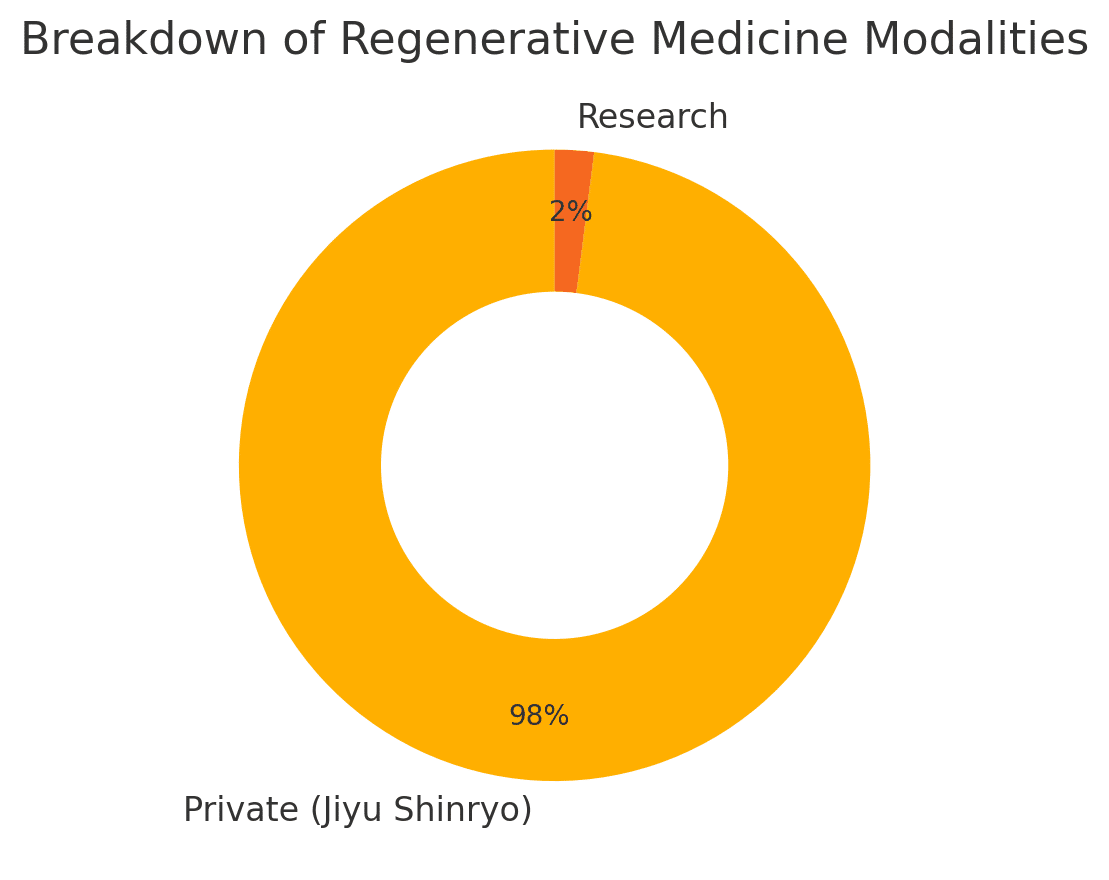
また、審査された計画の約25%は安全性や有効性を示す文献がほとんど引用されておらず、約30%では医師の専門分野と治療対象がミスマッチしていたと報告されています。
科学的エビデンスの不足
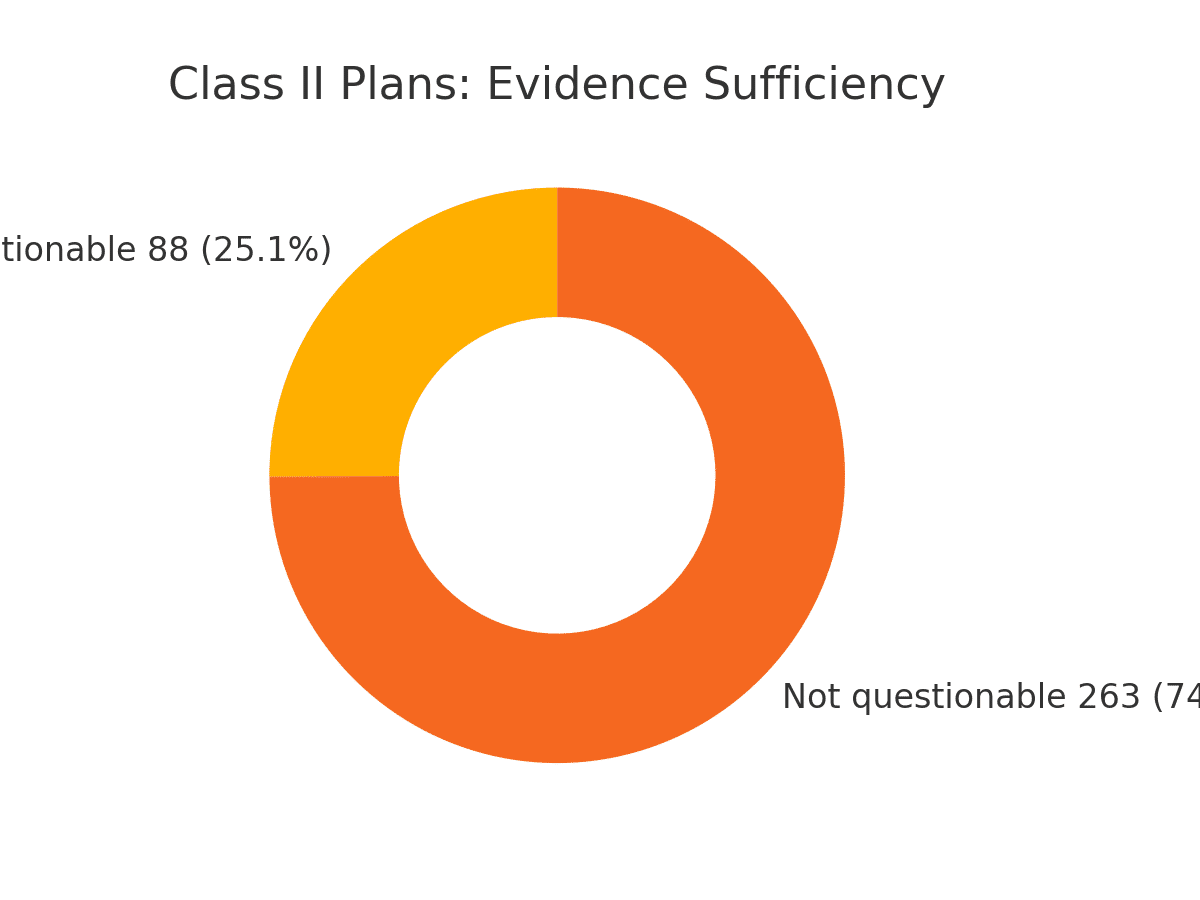
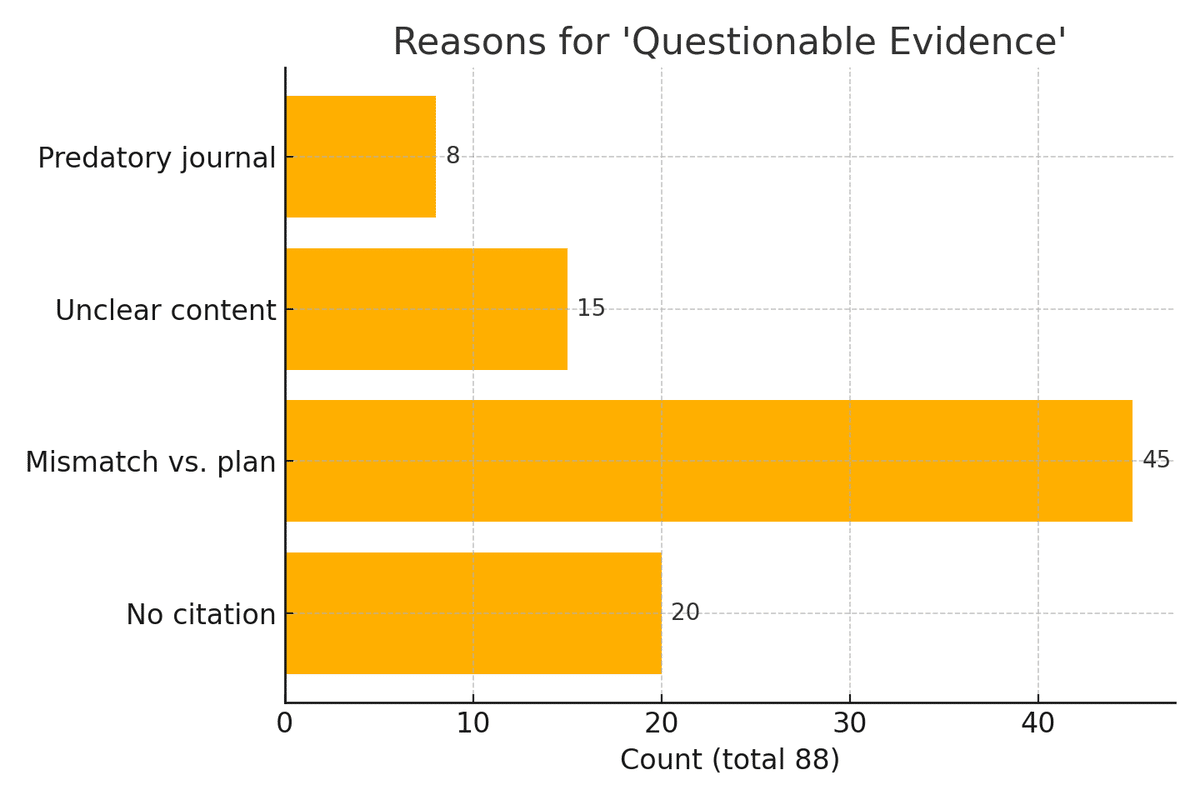
実際、届出された計画書の内容を分析した調査では、4分の1に当たる約25%の計画で安全性の科学的根拠が乏しいと判断されています。具体的には、「参考文献が一切引用されていない」(20件)、「文献はあるが今回の治療法や細胞・対象疾患とは異なる内容」(45件)、「文献内容が判別不能」(15件)、「査読のない質の低いジャーナル(ハゲタカ・ジャーナル)の論文を引用」(8件)といったケースが多数認められました。また約30%(100件以上)の計画で、治療内容と担当医師の専門分野にミスマッチ(例:産婦人科医が心筋梗塞の再生医療を実施)が推定されるなど、計画立案の妥当性にも疑問が生じています。こうしたデータは、自由診療下で提供されている再生医療には有効性・安全性の裏付けが弱いものが相当数含まれていることを示しています。効果が証明されていないだけでなく、理論的な安全性すら十分検証されていない治療が行われている実態は、患者にとって大きなリスクと言えます。
安全対策の不十分さ
自由診療のクリニックは一般的に規模が小さく、救急対応設備や専門スタッフが限られています。幹細胞点滴などの高度医療行為は急なアレルギーや塞栓症などを引き起こすことがあるため、治療中の適切な監視や緊急時の蘇生措置が不可欠ですが、それが十分でないまま提供されるケースがあります。また、治療後のフォローアップや副作用の報告が任意であるため、有害事象が過少に報告されるリスクも指摘されています。
費用が高く負担が大きい
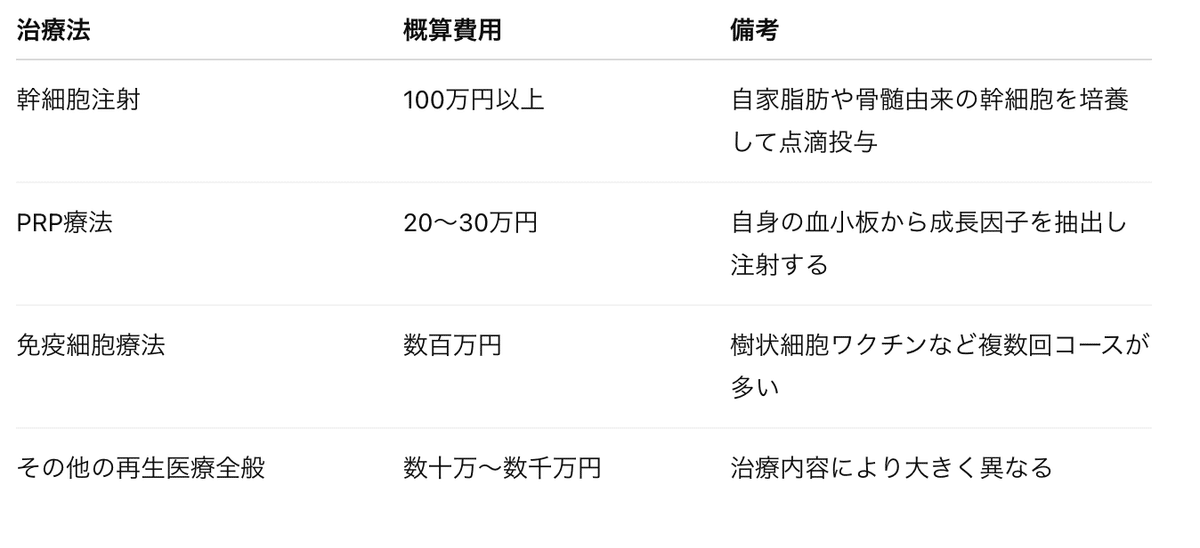
自由診療は保険適用外のため費用は全額自己負担です。例として、幹細胞注射は1回100万円以上、血小板由来成長因子(PRP)療法は1回20〜30万円、その他の免疫細胞療法は数百万円に上ることがあります。複数回コースとなることが多く、総費用が数百万円〜1,000万円を超えることもあり、経済的負担は小さくありません。下表は代表的な治療と概算費用をまとめたものです。
科学的エビデンスの不足
自由診療の再生医療は、有効性や安全性のエビデンスが十分に蓄積されていない段階で提供されることが多く、「画期的」や「先端医療」といった宣伝がなされます。研究段階の技術が商業化され、効果が確認されていないまま高額な費用を請求されることもあり、患者は治療効果を過度に期待しがちです。国内外の学会は、十分な臨床研究・治験を行い科学的根拠を蓄積することの重要性を指摘し、根拠の乏しい自由診療への安易な参加を控えるよう呼びかけています。
誇大広告と誤解を招く宣伝
自由診療の分野では「厚労省が認めた治療」「高い有効率」「海外で話題の最新治療」といった表現で患者の期待を煽る広告が散見されます。しかし、再生医療等安全性確保法のもとでは治療は承認ではなく届出制にすぎず、「承認済み」という表記は虚偽広告に当たります。日本再生医療学会は、根拠のない宣伝に惑わされないよう注意を呼びかけており、適切な情報提供と倫理的なマーケティングが求められます。
まとめと提言
自由診療の再生医療には先端医療への期待がある一方で、規制の隙間、医療安全体制の不足、高額な費用、科学的根拠の欠如、誇大広告といった多くの問題が潜んでいます。今回の事故は、未知のリスクがある治療を適切な準備や科学的裏付けなしに行う危険性を示しました。患者側は安易に「自分の細胞だから安全」と信じず、治療の根拠やリスク、費用対効果について十分な説明を受けることが重要です。医療機関や行政は、届け出制度の実効性を高め、審査委員会の独立性やモニタリング体制を強化し、エビデンスに基づく医療を推進する必要があります。
参考
- 厚生労働省:再生医療等安全性確保法に基づく緊急命令について(2025年8月29日) — 自家脂肪由来幹細胞を用いた自由診療中に患者が死亡したことを受け、治療の提供停止命令が出された経緯がまとめられている。
- テレビ朝日「スーパーJチャンネル」報道(2025年8月) — 点滴治療中に50代女性が急変し死亡した事例を伝えたニュース。
- 京都大学 iPS細胞研究所(CiRA)報告(2024年) — 届出された再生医療計画5,013件のうち自由診療がほとんどを占めることや、計画の25%に科学的根拠が乏しく、30%が専門分野とミスマッチであることなど、再生医療計画の質に関する調査。
- 日本再生医療学会「幹細胞を用いた自由診療について」(2023年) — 自由診療の再生医療は厚労省の承認を受けた治療ではなく、患者が全額費用を負担し、安全性の審査は行われても有効性は保証されないことを説明している。
- 日本再生医療学会プレスリリース「誇大広告への注意喚起」(2024年) — 再生医療は届出制であり、「厚労省が承認した治療」などの表現は虚偽広告に当たるとして一般市民に注意を促している。

